
Натрият (Na) е мек, сребристосив алкален метал с пореден номер 11, член на първа група в трети период на периодичната система, чието атомно тегло е 22,989768 u. Той е по-лек от водата, пластичен и с метален блясък. Предизвиква тежки химически изгаряния при допир. Проявява постоянна първа валентност. Той е един от най-активните метали, поради което не се среща в природата в свободно състояние. При контакт с въздуха се самозапалва, затова се съхранява в керосин или парафин.
Съединенията на натрия са познати и употребявани от човечеството от дълбока древност.Названието „натрий“ произлиза от древността, когато древните египтяни наричали съединенията на метала „натрон“, древните гърци – „нитрон“, а римляните и древните евреи – „нитер“.
Немският химик Мартин Клапрот нарича минералните алкални съединения „натрон“ или „натр“. Френският химик Лавоазие не поставя метала в своята „Таблица на простите тела“, защото смята, че най-вероятно е съединение, а не химичен елемент. Поради високата си реактивност, металът е изолиран сравнително късно, през 1807 г. от Хъмфри Дейви. Тогава той чрез електролиза на КОН отделя свободен К, а след няколко дни и Na от NaOH Нарича елементите „потасиум“ и „содиум“. През 1808 г. се появява названието „натрониум“, което Берцелиус съкращава до „натриум“. В българския език името „натрий“ произлиза от руското „натрий“. Така в различните езици елементът бива наричан „натрий“, „натриум“ или „содиум“.
Натрият е сребристосив нискотопим метал, който може да се реже с нож. Температурата му на топене е 97,8 °C, а на кипене – 882 °C. Има плътност 0,97 g/cm3. Поднесен в пламък, парите му излъчват жълт пламък, принадлежащ на D-линията на жълтото. Спектралните му линии се състоят от D1– и D2-линиите, със съответни дължини 589,597 nm и 589,000 nm.
Натрият е типичен алкален метал, член на 1-ва група, 3-ти период. Има електронната структура [Ne]3s1. Той е активен метал и реагира с повечето прости вещества и съединения, а под формата на катион се свързва с почти всички органични и неорганични аниони.Ниските стойности на йонизационна енергия и малката електроотрицателност определят метала като един от химически най-активните. При обикновени условия реагира с халогените, водорода, кислорода, сярата, повечето неметали, водата, оксидите и киселините. Разтваря се добре във вода и амоняк.Амонячният разтвор има син цвят и е силен редуктор:
Na2[NiII(CN)2]+2Na→��3Na4[Ni0(CN)4],
Mn20(CO)10+2Na⟶2Na[Mn−1(CO)5].
Възможно е и редуцирането на соли на тежки елементи до полианиони (Na4[Sb9]).
Първият промишлен способ за производството на натрий е от 19-и век
Na2CO3+2C⟶2Na+3CO
Натрият се получава чрез стопилка на свои соли или NaOH. От предложените методи за редукция и електролиза на NaOH, по-евтин се оказва електролизата на NaCl, смесен с малки количества CaCl2.
Много чист натрий се получава при разпадане на NaN3:
2NaN3⟶2Na+3N2
Металът натрий има широко приложение в различни отрасли на индустрията и бита. Той се използва за очистване на активни метали, като Zr и K, когато са течни. Подобрява кристалната структура и заглажда повърхността на металните сплави. Използва се като сушител на органични разтворители и за получаването на силни редуктори: NaH, NaOCH3, NaNH2 и окислители: Na2O2.
Натрият се използва при синтеза на различни вещества като каучук, багрилото индиго, витамин B12. Приложението му в атомните централи е свързано с добрата му топлопроводимост във втечнено състояние. Използва се и при производството на луминесцентни лампи.
Published: Feb 23, 2023
Latest Revision: Feb 23, 2023
Ourboox Unique Identifier: OB-1422284
Copyright © 2023
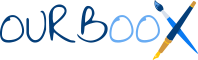








![{\displaystyle {\ce {Na2[Ni^{II}(CN)2] + 2Na ->[NH_{3}] Na4[Ni^{0}(CN)4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eb43287ce8374af602e45b7b7aba27fc6825cc98)
![{\displaystyle {\ce {Mn^{0}2(CO)10 + 2Na ->2Na[Mn^{-1}(CO)5]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aa5d94f599c40016a2d4fbd6596889d0d4b8ce6a)

