by Levchenko Larisa
Copyright © 2020
Стан певної маси газу визначається трьома макроскопічними параметрами — тиском p, об’ємом V і температурою T. Однак багато процесів у газах, що відбуваються в природі або здійснюються в техніці, припустимо розглядати (приблизно) як процеси, у яких змінюються лише два з них.
Особливу роль у фізиці й техніці відіграють так звані ізопроцеси.
Ізопроцесами називаються процеси, що протікають із певною масою газу за постійного значення одного з трьох параметрів — тиску, об’єму або температури
- Закон Бойля-Маріотта
Ізотермічний процес — це процес, перебіг якого відбувається за постійної температури (від грец. «термо» — тепло).
Зміну тиску й об’єму газу за постійної температури називають ізотермічним процесом.
Досвід показує: якщо стискати газ за постійної температури, тиск зростає обернено пропорційно об’єму. Це означає, що під час ізотермічного процесу тиск газу обернено пропорційний його об’єму: за
У середині ХVІІ ст. два фізики англієць Р. Бойль і француз Е. Маріотт, експериментально вивчивши ізотермічний процес в ідеальному газі даної маси, відкрили закон, який назвали законом Бойля-Маріотта.
У разі ізотермічного процесу тиск певної маси газу обернено пропорційний його об’єму: або



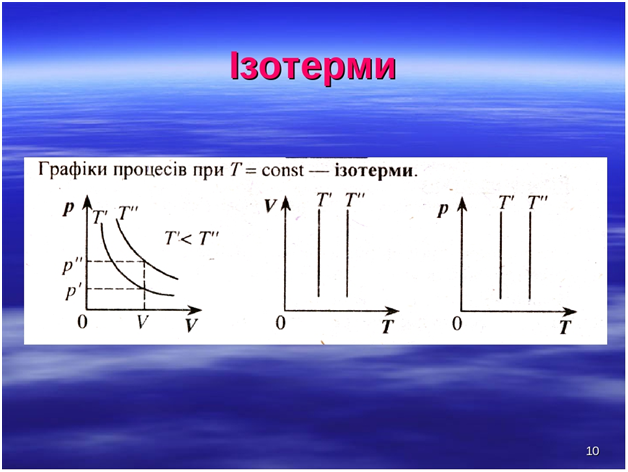
Графік залежності p (V) за T=const називають ізотермою.
Цей графік показує, що за постійної температури тиск газу обернено пропорційний його об’єму.
Реальний процес у реальному газі можна вважати ізотермічним, якщо він відбувається дуже повільно, так що зміною температури газу за деякий незначний інтервал часу можна знехтувати.
2. Ізобарний процес— це процес, який відбувається за постійного тиску (від грец. «барос» — тиск).
Зміна об’єму й температури газу за постійного тиску називається ізобарним процесом.
Під час ізобарного процесу об’єм газу прямо пропорційний його абсолютній температурі: за . Це співвідношення називають законом Гей-Люссака— на честь французького вченого, який відкрив його на початку ХІХ ст.
Закон Гей-Люссака дозволяє пов’язати значення об’єму і температури певної маси газу у двох різних станах, якщо тиск газу в обох станах однаковий. Позначимо V1 і T1 значення об’єму й температури газу в стані 1, а V2 і T2 — у стані 2.


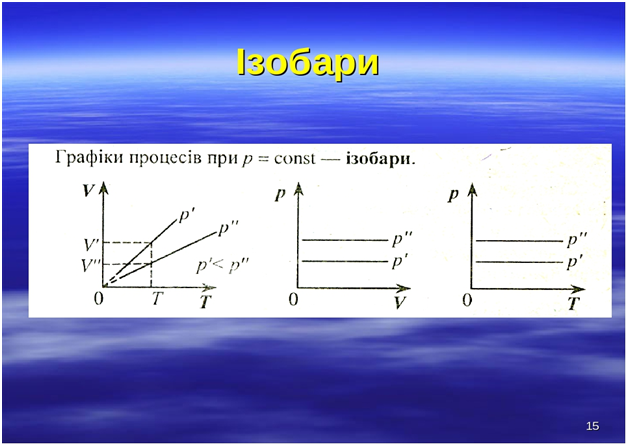
Цей графік називають ізобарою. Він показує, що за постійного тиску об’єм газу прямо пропорційний його абсолютній температурі.
З позиції МКТ закон Гей-Люссака можна обґрунтувати: у разі ізобарного підвищення температури збільшується середня кінетична енергія молекул газу та їх середня швидкість, що пов’язано зі збільшенням довжини вільного пробігу молекул, тобто простору між ними. Тому у разі ізобарного розширення або стискання газу об’єм змінюється відповідно до зміни температури.
Слід ще раз підкреслити: якщо газ вільно змінював свій об’єм і при цьому зовнішні сили, які чинять на нього тиск, залишалися незмінними, то в ньому відбувався ізобарний процес.
3. Ізохорний процес— це процес, який протікає за постійного об’єму (від грец. «хорос» — об’єм).
Зміну тиску й температури газу за постійного об’єму називають ізохорним процесом.
Досвід показує: якщо нагрівати газ за постійного об’єму, тиск газу збільшуватиметься прямо пропорційно абсолютній температурі.
Це означає, що під час ізохорного процесу тиск газу прямо пропорційно його абсолютній температурі: за
Залежність тиску газу від температури було досліджено наприкінці XVIII ст. французьким ученим Шарлем, тому наведене співвідношення називають законом Шарля.
У разі ізохорного процесу тиск певної маси газу прямо пропорційний його абсолютній температурі:


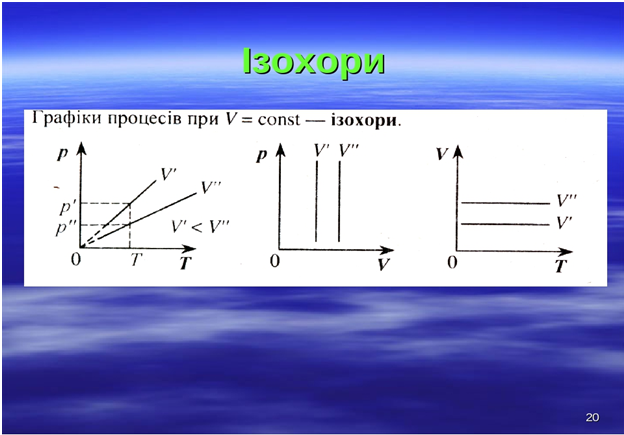
Цей графік показує, що за постійного об’єму тиск газу прямо пропорційний його абсолютній температурі.
З позиції МКТ закон Шарля можна пояснити так: якщо збільшувати температуру газу, не даючи йому розширюватись, тобто помістивши в закриту посудину, то із зростанням середньої кінетичної енергії його молекул їхні удари об стінки посудини будуть посилюватись, тобто тиск газу збільшуватиметься.
Домашнє завдання:
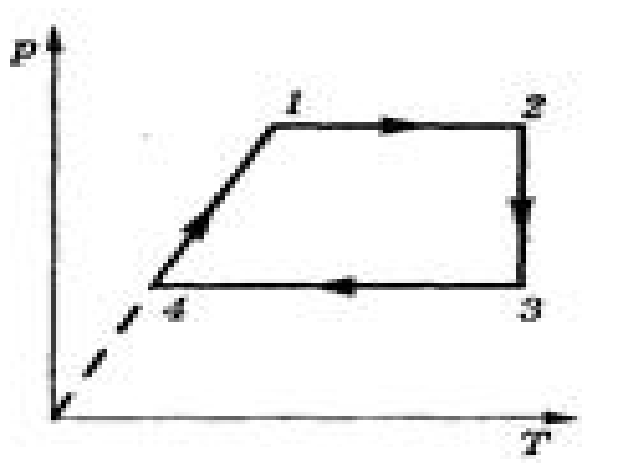
- Побудуйте графіки процесу, що відбувається з ідеальним газом (див. малюнок) в координатах р, V і V, Т. Маса газу постійна.
- Нагрівається або охолоджується газ, що розширюється за законом: a) p V 2= const; б) р = const; в) p/V = const?
- У посудині об’ємом V = 1,0 л знаходиться азот масою m = 0,28 г. Азот нагрітий до температури t = 1500°C, при якій 30% всіх молекул азоту дисоціюють на атоми. Визначте тиск р в посудині.
Published: Mar 5, 2020
Latest Revision: Mar 5, 2020
Ourboox Unique Identifier: OB-743245
Copyright © 2020