Лабораторна робота №5
Дослідне підтвердження закону Бойля-Маріотта
Мета роботи: дослідити, як змінюється об’єм повної маси газу (при сталій температурі) із зміною тиску, і встановити співвідношення між ними.
Прилади і обладнання :
Скляний циліндр висотою 40 см з водою (або мензурка)
Скляна трубка довжиною 40-50 см, закрита з одного кінця
Вимірна лінійка з міліметровими поділками
Барометр БР – 52 (один на групу)
Штатив універсальний
Загальні теоретичні положення
Для опису властивостей газів користуються трьома макропараметрами, які однозначно визначають стан газу та знаходяться простим вимірюванням за допомогою приладів, це тиск – p , абсолютна температура – T і об’єм газу – V . Значення таких величин визначається спільною дією великої кількістю молекул, тому їх називають макроскопічними (від грецького ‘макрос’ – великий ). Тиск вимірюють барометром, температуру – термометром, а об’єм – лінійкою або мензуркою.
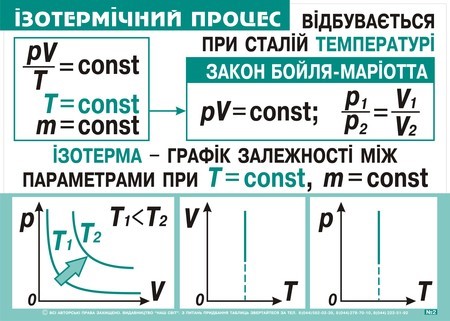
Процес у газі, який відбувається при постійній температурі (T = const ), називають ізотермічним, а його графік – ізотермою. Залежність між тиском p газу і його об’ємом V при постійній температурі дослідним шляхом вперше встановили Р. Бойль і Є. Маріотт.
Закон Бойля-Маріотта визначає те, що якщо маса газу у системі не змінюється (замкнена система), то добуток тиску газу на його об’єм є постійна величина для будь-якого стану газу при ізотермічному процесі.
Це означає, що при зменшенні об’єму газу тиск зростає, а при його збільшенні тиск спадає. При ізотермічному стисканні газу його частинкам надається менший об’єм і, тому, вони частіше стикаються зі стінками посудини, що призводить до збільшення тиску газу. При ізотермічному розширенні газу все відбувається навпаки.
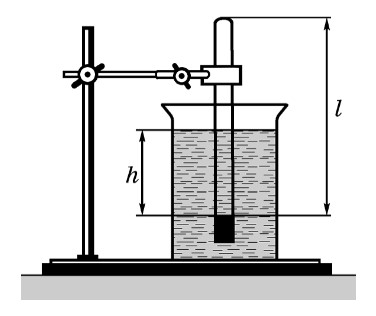
Закон Бойля-Маріотта можна перевірити за допомогою обладнання.
Опустити відкритим кінцем вниз трубку у скляний циліндр висотою 40 см з водою і закріпити її у штативі. Повітря в трубці буде під тиском, який дорівнює атмосферному H плюс гідростатичний тиск стовпчика води висотою h . (Для спрощення розрахунку атмосферний тиск і тиск стовпчика води доцільно вимірювати в мм рт. ст.).
Густина води в 13,6 рази менша за густину ртуті, тому стовпчик висотою h мм створює такий самий тиск, як стовпчик ртуті висотою
Повітря в трубці буде під тиском:
де Н – атмосферний тиск, виражений в мм рт. ст.;
h – різниця рівнів води, виміряна в мм, у циліндрі і в трубці
Порядок виконання роботи
Виміряйте барометром атмосферний тиск Н в мм рт. ст.. ( Під таким тиском знаходиться повітря в трубці до її занурення у воду ).
Опустіть у воду трубку відкритим кінцем вниз на максимальну глибину. Виміряйте довжину стовпчика L повітря в трубці і різницю рівнів води в ній і в циліндрі – h . Щоб зручніше було визначити довжину стовпчика L повітря в трубці, один раз виміряйте лінійкою довжину трубки, яку занурюєте в воду, та віднімайте від цього значення довжину стовпчика води, що в ній знаходиться у нижній її частині.
Повторіть вимірювання L і h для двох менших глибин занурення трубки;
Обчисліть за формулою:
p=H+h/13.6
для всіх трьох дослідів, порівняйте їх між собою, зробіть висновок;
Результати вимірювань і обчислень запишіть у таблицю 1.


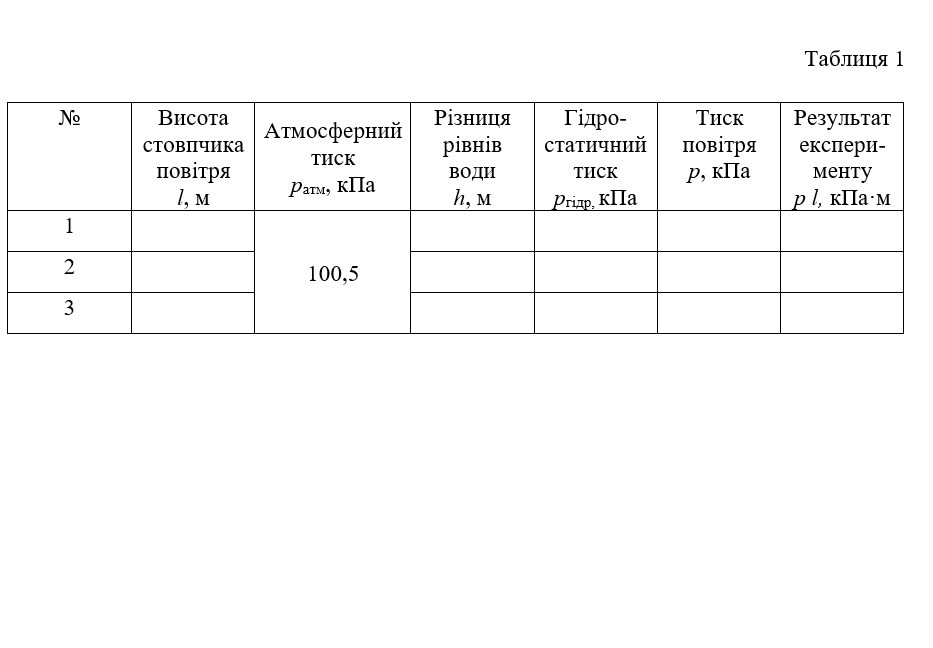
Аналіз експерименту та його результатів
Проаналізуйте експеримент і його результати. Сформулюйте висновок, у якому зазначте:
1) який закон ви експериментально перевіряли;
2) які величини для цього вимірювали;
3) яким є результат перевірки;
4) у чому причина похибки;
5) вимірювання якої величини дає найбільшу похибку.
Лабораторна робота №6
Визначення коефіцієнта поверхневого натягу рідини
Мета роботи: виміряти поверхневий натяг води методом відриву крапель.
Обладнання: штангенциркуль, медичний шприц об’ємом 2 мл без голки, зубочистка, склянка з дистильованою водою.
Теоретичні відомості
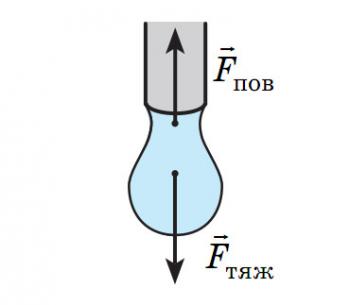
У ході повільного витікання рідини з тонкої вертикальної трубки на кінці трубки утворюється крапля (див. рисунок).
Відрив краплі відбувається в той момент, коли сила тяжіння зрівнюється із силою поверхневого натягу, що діє на краплю вздовж кола шийки краплі: Fпов=Fтяж або m0g=σl, де m0 — маса краплі; σ — поверхневий натяг рідини; l = πd — довжина кола (d — внутрішній діаметр трубки).
Масу краплі можна знайти за формулою: m0=V0ρ=Vρ/N, де ρ — густина рідини; V — об’єм рідини, що витекла; N — кількість крапель. Отже, вимірявши внутрішній діаметр трубки d і порахувавши кількість N крапель, що утворилися під час витікання рідини об’ємом V, можна обчислити поверхневий натяг рідини:
σ=(ρVg)/(Nπd)
Хід роботи
- Виміряйте діаметр вихідного отвору шприца.
- Наберіть у шприц 2 мл води. Повільно натискаючи на поршень і рахуючи краплі, викапайте воду у склянку.
- Повторіть дослід ще 3 рази.
- Дані дослідів запишіть в таблицю 2


Published: Jan 19, 2023
Latest Revision: Jan 19, 2023
Ourboox Unique Identifier: OB-1407540
Copyright © 2023