Литий:
Литият е химичен елемент със символ Li и атомен номер 3.
Литиева основа- (2LiOH)
2Li + 2HOH ->2LiOH + H2
Литият реаргира с вода подобно на натрия.
Li+ H2O->LiOH + H2 ,
.

Физични свойства:
Лития е мек сребристо-бял алкален метал.
При стандартни условия е най-лекият метал и най-лекият твърд елемент. Подобно на всички алкални метали, литият е силно реактивоспособен и затова се съхранява под петрол. Той е с метален блясък, но изложен на въздух, бързо потъмняв. Литият е достатъчно мек, за да бъде срязан с нож. Когато се нареже, той има сребристо-бял цвят, който бързо се променя до сиво, тъй като се окислява до литиев оксид.

Химични свойства:
Характерни химични съединения на алкалните елементи:
Формулa на хидридите – LiH
Формула на оксидите – Li2O
Формули на основите – LiOH
Състояние на веществото – твърдо
Строеж на веществото – йонен
Свойство на атома да се превръща в йон:
Li-e– -> Li+
Брой протони в ядрото на атомите – 3
Относителна атомна маса (Ar)– 6,9
Когато бъдат поставени върху пламък, литиевите съединения оцветяват пламъка в розово-червеникав цвят, но когато изгарят силно, пламъкът става сребрист. Литият се запалва и гори в среда от кислород и когато е изложен на вода или водни пари.

Съединения:
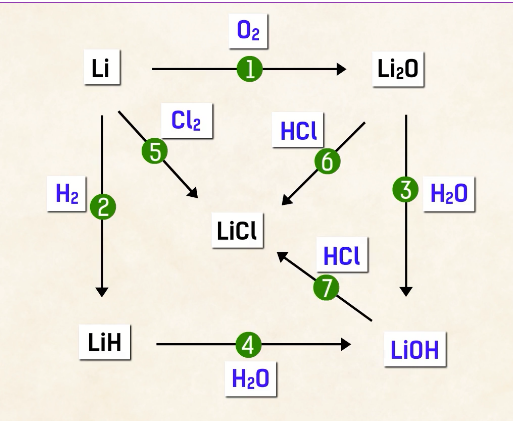
1) От метал трябва да получим оксид , металът трябва да взаимодейства с кислород.
2) Трябва да получим хидрид от литий , като взаимодейства метала с кислород. Избран е простото вещество водород.
3) Съединението , което трябва да се получи , трябва да бъде един път от оксида и един път от хидрида. Единствената реакция , която знаем за хидридите е с вода за получаване на съответната основа и водород. Основните оксиди: дилитиев оксид , образуват основни хидроксиди или основи и ще бъде литиев хидроксид. Получаваме литив хидроксид от оксида , чрез взаимодействие с вода.
4) Трябва взаимодействие с вода , за да се получи литиева основа.
5) Получаване на солта литиев хлорид от метала литий , чрез взаим одействие с хлор или солна киселина.
6) От литиев оксид , сол хлорид , като основните оксиди взаимодействат с киселини и за да е солта хлорид , киселината трябва да съдържа хлор и такава е солната киселина (HCI).
7) От литиева основа да получим литиев хлорид. Основите се неутрализират с киселини и отново е солна киселина.
Съединения с Оксид, пероксид и хидроксид:
Литиевият пероксид (Li2O2) се получава при взаимодействие на етанолов разтвор на LiOH с H2O2. Първоначален продукт е литиевият хидрогенпероксид, който се разпада поради своята нестабилност:
Той се използва в космическите кораби за получаване на кислород:
Литиевият хидроксид (LiOH) е твърдо, бяло, силно хигроскопично вещество с ниска температура на топене. Получава се при взаимодействието на Li2O с вода.

Получаване на алкални хлориди:
-
2Li + CI2 -> 2LiCl
-
2Li + 2HCI -> 2LiCl + H2 (като газ)
-
Li2O + 2HCI -> 2LiCl + H2O
-
LiOH + HCI -> LiCl + H2O
Производство:
Благодарение на неговата разтворимост като йон, литият присъства в морската вода и тя е главният източник за получаването му.

Приложение:
Литият и неговите съединения имат няколко индустриални приложения включително при производството на топлоустойчиво стъкло и керамика, литиеви смазочни масла, добавка при производство на желязо , стомана , алуминий и литийево-йонни батерии. Съединения на лития се използват във вентилационните системи на космически кораби, подводници, за надуване на спасителни лодки, в стъкларската (за специални оптически стъкла, използвани при работа с рентгенови лъчи) и керамичната индустрия.
Литият присъства в биологичните си в малки количества, но неговите функции са неясни. Литиевите соли (LiCO3) се използват в производството на лекарства при лечението на биполярното разтройство.

Интересно:
„Едно от най-големите находища на литий в света е до Лозница (в Сърбия) и това може да ни донесе богатства“.
Всъщност литият е един от най-разпространените елементи в природата, но не се намира концентриран в находища. Засега добивът му е изгоден в пустините на Латинска Америка, там се изтегля като разтвор на литиев хлорид, водата се изпарява в солници и остатъкът се обработва. Този тип производство не замърсява с отрови. Ако литият поскъпне достатъчно, ефикасни ще станат и други методи, включително изтеглянето му от морска вода или копаене на подземни находища.

Published: Mar 12, 2023
Latest Revision: Mar 12, 2023
Ourboox Unique Identifier: OB-1428280
Copyright © 2023